爱姆斯坦首席科学家王小方博士研究发现,人胚胎干细胞来源的间充质干细胞(hESC-MSC)比成人组织来源的MSC具有更强的免疫调节功能和更低的免疫原性潜力。与骨髓来源的MSC相比,hESC-MSC产生的炎性细胞因子较少,表达的MHC II类分子较少。它可预防免疫介导的炎症,阻止疾病进一步进展,并通过修复和再生促进神经元的恢复。
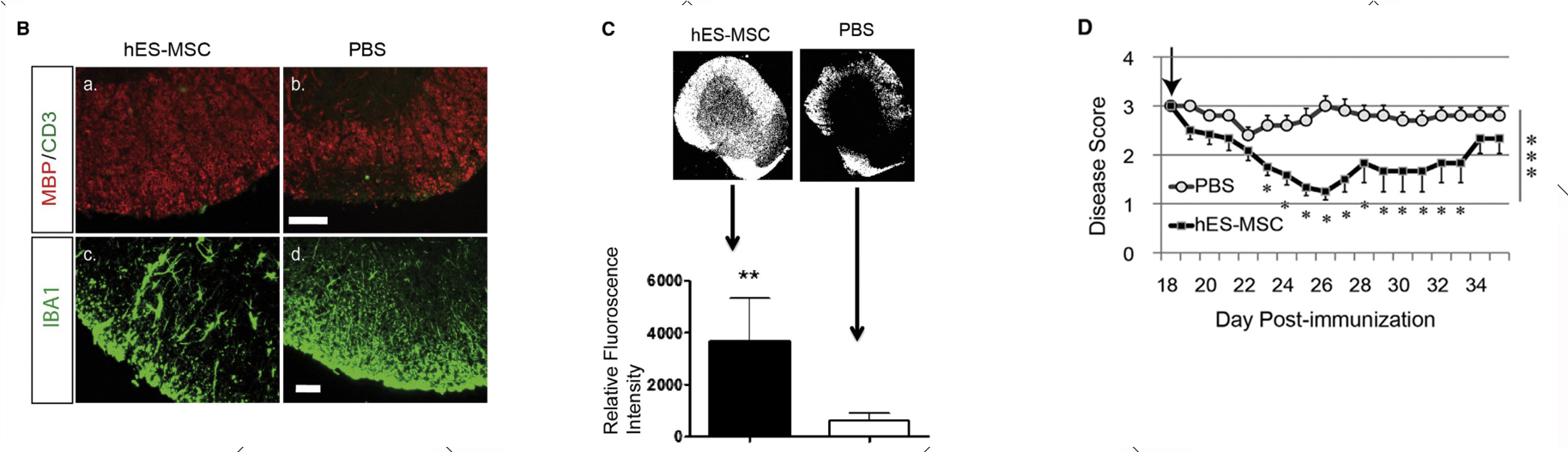
2014年,王小方博士在 Stem Cell Reports上发表的文章[1]指出人胚胎干细胞来源的间充质干细胞(hES-MSCs)在多发性硬化经典模型——EAE(Experimental autoimmune encephalomyelitis)的治疗方面优于骨髓间充质干细胞(BM-MSCs)。hES-MSCs处理的小鼠可以防止脱髓鞘(原文图1B和1C)。无论是预防性还是治疗性给药,hES-MSCs都能减轻小鼠的EAE疾病评分(评分越高疾病越严重)(原文图1D)。
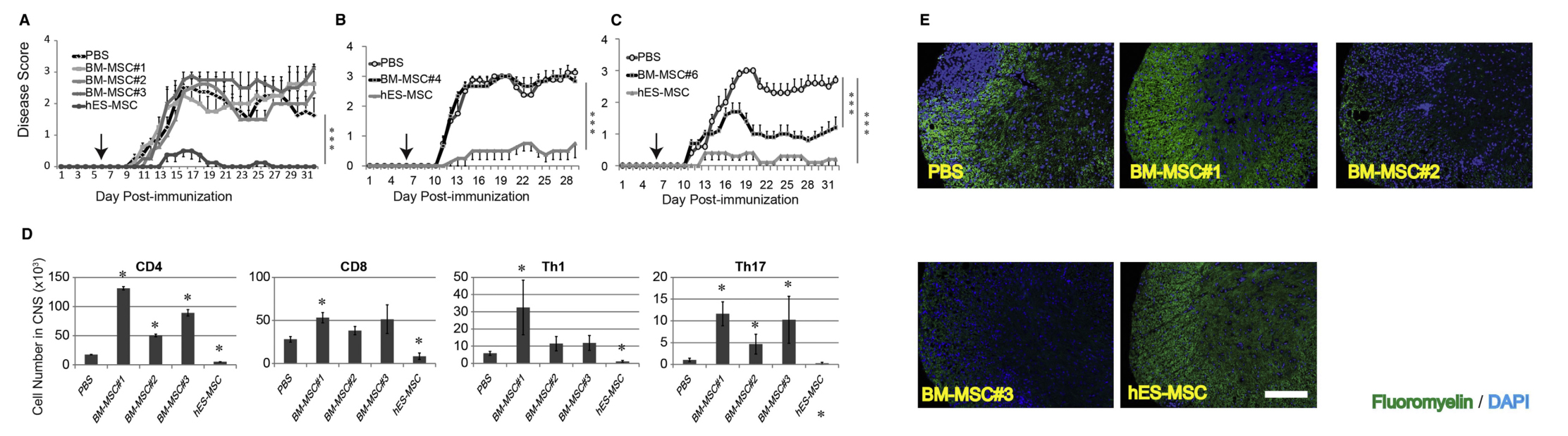
hES-MSCs比BM-MSC具有更强的EAE抑制作用。与不同供体来源的BM-MSCs相比,hES-MSCs可以显著降低EAE的疾病评分(评分越高疾病越严重)(原文图3A-3C),hES-MSCs组中枢神经系统中CD4+、 CD8+、Th1和Th17细胞浸润明显减少(原文图3D),PBS和BM-MSCs组小鼠出现严重的脱髓鞘(原文图3E)
2015年,王小方博士在Stem cells上发表的研究发现[2],T-MSCs在体外表现出有效的免疫调节活性,因为它们可以显著抑制共培养的T和B淋巴细胞的增殖。(原文图2A-2D)
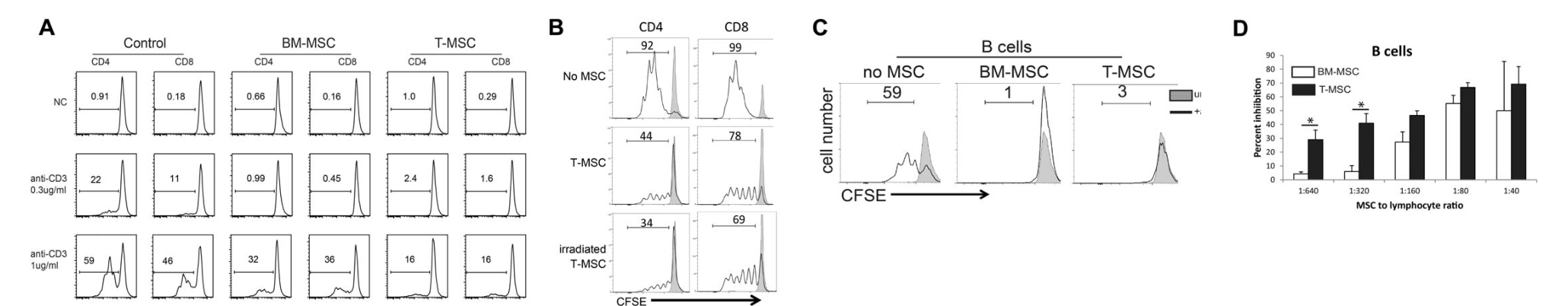
图:hES-MSCs优于成体 MSC,可产生较少的促炎症因子(原文图3A、3C),并且比BM-MSC具有更低的免疫原性
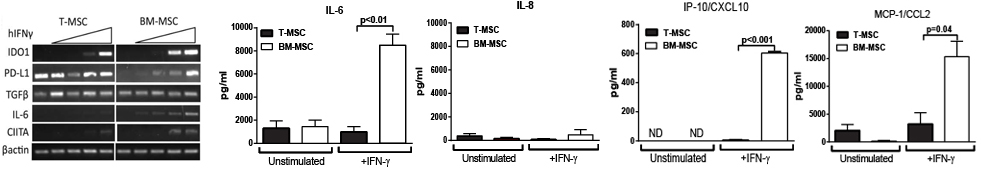
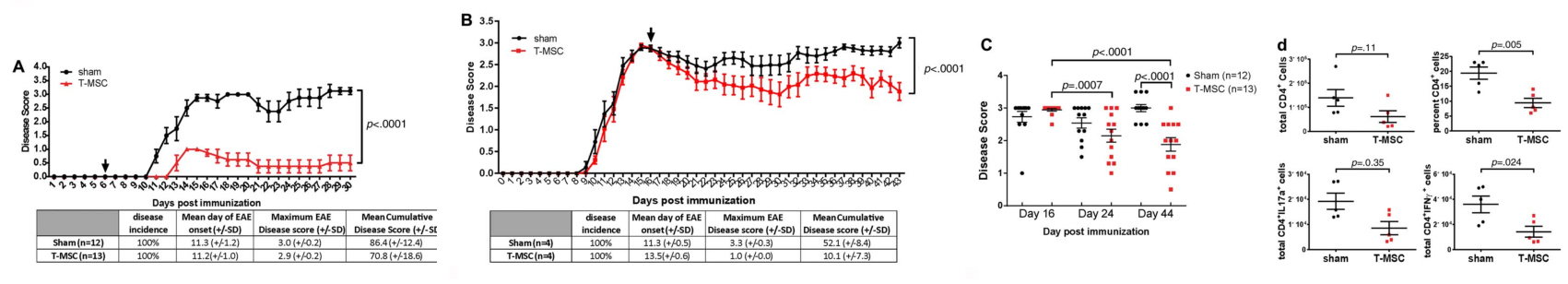
图:T-MSCs可预防小鼠EAE的发作并降低其严重程度(原文图5)
目前,基于王小方博士的研究,非临床研究充分证实了按现有生产工艺和质量管理体系制备的制剂成品对MS具有显著的治疗效果并具有很好的安全性。